상세 컨텐츠
본문
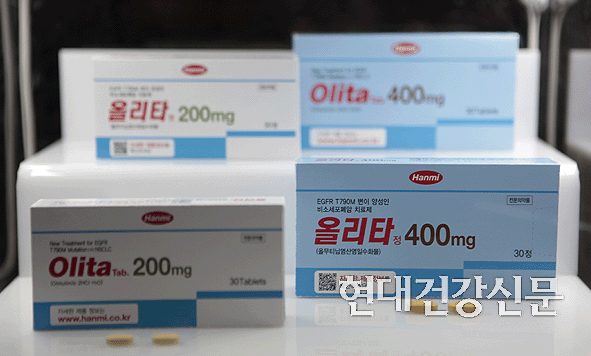
[현대건강신문=여혜숙 기자] 임상시험 도중 심각한 피부독성부작용이 발생한 한미약품의 폐암 신약 ‘올무티닙’(제품명 올리타 정)이 국내 판매중단은 면했다. 중증피부이상반응에도 불구하고 말기 폐암환자에게 사용할 만한 유효성은 충분하다는 판단이다.
4일 식품의약품안전처는 중앙약사심의위원회를 열고, 올무티닙의 제한적 사용을 허용했다.
식약처는 기존 치료제로는 효과가 없어 더 이상 치료방법이 없는 말기 폐암환자를 대상으로 허용이 허가된 항암신약인 한미약품 올리타정에 대해 의사의 전문적 판단하에 중증피부이상반응의 부작용이 생길 수 있음을 환자에게 자세히 설명하고 복용에 대한 동의를 받아 제한적으로 사용하는 것으로 결정했다고 밝혔다.
또한 정식 처방을 받아 해당 의약품을 복용한 모든 환자에 대해 집중적으로 전수 모니터링하기로 하고 의사 및 환자에 대해 중증피부이상반응 등 발생 가능성 및 주의사항에 대해 집중교육 하기로 했다.
식약처 관계자는 “이번 결정은 안전성 정보와 중앙약사심의위원회의 자문결과, 대체 치료방법이 없는 환자에게 치료기회 제공 등을 종합적으로 고려한 것”이라고 밝혔다.
한편, 한미약품이 개발한 올무티닙은 기존 치료에 실패한 말기 비소세포폐암환자를 대상으로 폐암치료제로, 다국적 임상시험 진행 중 중증피부 이상반응 3건(‘독성표피괴사용해’ 사망 1명 포함해 2건, 스티븐스존슨증후군 1건)이 발생했다. 이와 관련해 식약처는 지난 30일 안전성 서한을 배포하고 신규투약을 금지한 상태다. 그러나 식약처는 지난 4월 첫 사망 사례를 보고 받고도 5월 신속심사를 통해 국내 시판 허가를 내줬다는 비난을 받고 있다.
'약_건강' 카테고리의 다른 글
| 미국 FDA 금지한 돔페리돈 성분 소화제, 국내 임산부에게 7만8천여건 투여 (0) | 2016.10.07 |
|---|---|
| 우상호 대표 “늑장공시 의혹 한미약품 사실이면 일벌백계해야” (0) | 2016.10.06 |
| [건강포토] 공시지연 의혹 해명하는 한미약품 이관순 대표 (0) | 2016.10.02 |
| 한미약품 ‘올리타’ 설상가상...중증피부이상반응으로 1명 사망 (0) | 2016.09.30 |
| 베링거인겔하임, 올무티닙에 대한 권리 한미약품에 반환 (0) | 2016.09.30 |